12 maggio 2019
Walter Borsini
Presentazione al Convegno:
La Patologia Degenerativa Encefalica
Villa Ulivella e Glicini , Firenze ,
13 marzo 2019
Patologia Degenerativa Encefalica nell’ età adulta e anziana
Inquadramento clinico
INTRODUZIONE
Come tutti sappiamo , è possibile invecchiare bene , e sappiamo anche che alcuni comportamenti aiutano a farlo.
Ecco tre buone regole:
1.Alzarsi da tavola con un po’ di fame
2.Molto movimento, che sia piacevole ed efficace a smuovere i parametri cardiocircolatori
3.Un buon medico di base (aiutato da specialisti, se necessario) per la prevenzione delle malattia in particolare cerebrovascolari
Con normal brain aging intendiamo l’ invecchiamento, con una buona qualità della vita personale e di relazione, anche in età avanzata, più prosaicamente chiamato anche invecchiamento senza demenza
Tuttavia ci sono molti ostacoli che il nostro cervello incontra sulla strada di un buon invecchiamento.
Io parlerò di alcuni di questi ostacoli , dividendo la mia esposizione in due parti.
Dapprima, come dice il titolo, faremo una panoramica sui cambiamenti inevitabili che accompagnano l’ invecchiamento, anche quello normale, senza alterazioni cognitive significative; poi parleremo dei principali processi patologici, cioè di quelli vascolari e degenerativi, che sono all’ origine della maggior parte delle demenze; e infine parleremo di alcune cause più particolari di demenza, come l’ idrocefalo normo-teso, o di situazioni che comunque entrano in diagnosi differenziale con le demenze, come il Delirium.
I CAMBIAMENTI DEL CERVELLO DURANTE L’INVECCHIAMENTO
I processi patologici a cui accenneremo brevemente esordiscono in maniera subdola , sub-clinica , in soggetti perfettamente normali anche sul piano cognitivo e motorio, si sviluppano lentamente, insidiosamente, arrivando negli anni, ma non in tutti i soggetti , a quadri di evidente compromissione cognitiva o del cammino.
Con l’ età, il cervello va incontro a diversi cambiamenti, le modifiche strutturali correlate all’ invecchiamento stesso e processi degenerativo – vascolari patologici, spesso subclinici e inapparenti
Molti di questi cambiamenti possono essere osservati alla Risonanza Magnetica, già molti anni prima che essi provochino sintomi clinicamente rilevabili, e quindi anche in soggetti che sono ancora asintomatici e cognitivamente normali
Ci sono importanti differenze inter-individuali
•nella precocità di comparsa,
•nella velocità di progressione
•nelle conseguenze clinico-cognitive a parità di danno strutturale
Quindi, oltre l’ età, molti altri fattori causali/protettivi (non ancora sufficientemente noti) intervengono a determinare il quadro clinico in ogni singolo paziente.
Che cosa vediamo a livello micro-strutturale nel cervello che invecchia?
Ecco alcuni esempi:
1.Perdita di consistenza, gliosi, demielinizzazione, perdita di assoni
2.Lesioni infartuali, distruttive, lacunari o estese
3.Micro-emorragie
4.Perdita di volume globale, atrofia cortico-sottocorticale regionale, degenerativa e/o vascolare; l’ atrofia interessa anche la sostanza bianca - e non solo la sostanza grigia -. L’ atrofia della sostanza bianca è critica perchè estese reti neurali la attraversano, che sono necessarie per molti processi di ordine superiore inclusi attenzione, funzioni esecutive, funzionamento visuale/non verbale, e in generale per la velocità dei processi stessi. La riduzione della integrità della sostanza bianca pre-frontale è uno dei meccanismi sottostanti il rallentamento delle percezioni e della memoria episodica nell’ anziano.
5.Accumuli di amiloide, proteina tau, sinucleina. In particolare recenti acquisizioni suggeriscono che la patologia della proteina tau preceda di anni l’ accumulo di amiloide dell’ Alzheimer, anche nelle strutture sottocorticali , come l’ ippocampo.
6.Altri processi non ancora noti, non ancora visibili al neuroimaging, ma che hanno a che fare con la struttura microscopica e cellulare dei network neurali Questo ultimo punto è particolarmente importante , anche se è quello che conosciamo meno, perché probabilmente è quello che condiziona le differenze sintomatiche tra soggetti che apparentemente hanno analogo carico lesionale strutturale al neuroimaging.
Come suddividiamo la compromissione cognitiva ? Un soggetto può essere:
•Cognitivamente integro
•Con Compromissione cognitiva lieve (Minimal Cognitive Impairment o MCI)
•Con Demenza, quando la compromissione cognitiva impatta in maniera significativa seppure parziale sulle usuali attività quotidiane e quindi sull’ autonomia sociale e/o personale. Di solito nella demenza, oltre al calo di memoria sono interessati altri domini e competenze cognitive «focali», come il linguaggio o le prassi. La persona non riesce a trovare strategie compensative ai suoi deficit, sufficienti a preservarne appunto una soddisfacente autonomia sociale e personale
I soggetti con demenza possono avere una compromissione lieve , moderata o severa.
Quelle riportate nella TAB. 1 sono le malattie che più frequentemente possono evolvere a Demenza. E’ bene distinguerle in base alla frequenza con cui al disturbo cognitivo si associa un disturbo motorio.
TAB. 1 Cause di Demenza
Demenze associate a disturbi motori, e del cammino
•Forme vascolari
•Forme degenerative come la Demenza Fronto-Temporale, che esiste in diverse varietà, con maggior compromissione comportamentale, del linguaggio o motoria , e raramente anche associata a malattia del secondo motoneurone
•Parkinson Demenza (Malattia dei Corpi di Lewy)
•Altre forme extrapiramidali (Paralisi Sopranucleare Progressiva o PSP, Atrofia Multisistemica o MSA)
Demenze di solito non associate a disturbi motori, del cammino
•Alzheimer
ENCEFALOPATIA VASCOLARE E ENCEFALOPATIA DEGENERATIVA
Possiamo vedere adesso più in dettaglio alcune delle alterazioni patologiche cui l’ encefalo va incontro nell’ invecchiamento.
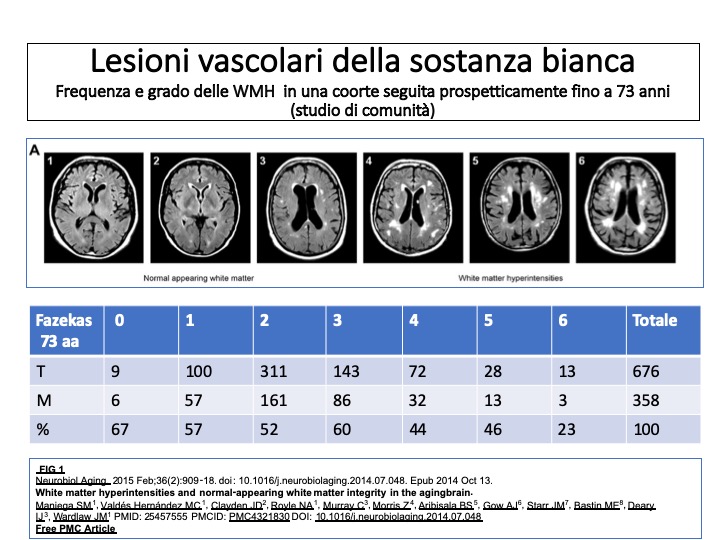
Come abbiamo visto molto frequenti sono le alterazioni della sostanza bianca su base vascolare-ischemica. Queste appaiono come iper-intensità della sostanza bianca encefalica alla RM. Nella popolazione generale in uno studio di comunità su quasi 700 persone seguite prospetticamente fino all’ età di 73 anni, che si è occupato delle iper-intensità della sostanza bianca, la cui origine è di solito vascolare (FIG. 1). A 73 anni solo il 16% è sostanzialmente del tutto indenne da queste alterazioni, mentre il 17% le presenta in modo discreto o severo. Il 67% dei soggetti presenta alterazioni lievi.
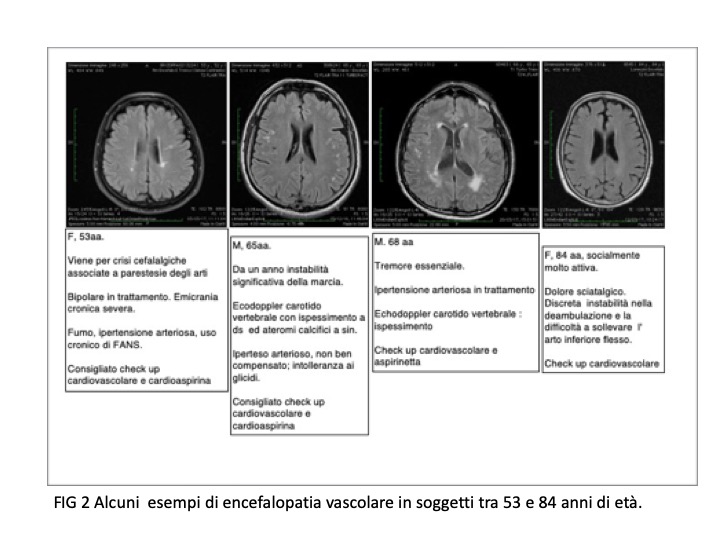
Naturalmente queste alterazioni possono comparire anche molto prima dei 70 anni, come si vede nella FIG 2 , di casi seguiti personalmente, figura che ci vuole mostrare proprio che l’ età d’ insorgenza di questa alterazioni
presenta importanti differenze inter-individuali; così possiamo trovarle in soggetti di 50 ma possono essere ancora assenti in alcuni soggetti di 85 anni
Questo tipo di alterazioni resta asintomatico per anni o decenni, tanto che spesso vengono scoperte per caso. Possono passare anni , qualche volta decenni, prima che esse, accumulandosi nel cervello, finiscano per creare una compromissione significativa delle funzioni corticali cognitive o dell’andatura.
Nella figura successiva (FIG. 3) possiamo vedere le neuro-imagini di un paziente che comincia presentare i primi disturbi cognitivi su base cerebro-vascolare intorno ai 74 anni. La diapositiva mostra, oltre alle alterazioni ischemiche di cui stiamo stiamo parlando, anche una micro-sanguinamento, che invece appare nero in alcune particolari sequenze della RM (Gradient Echo) .
.
Una breve sintesi sulla patologia vascolare ischemica e micro-emorragica che può compromettere il normal brain aging:
L’ encefalopatia vascolare non è un’ emergenza; di per sé, in assenza di altri indicatori clinici, non predice eventi imminenti
•Le alterazioni cerebrali vascolari asintomatiche (infarti silenti, leuco-encefalopatia, lesioni iperintense della sostanza bianca, microsanguinamenti) possono precedere lo stroke o il declino cognitivo di decenni.
•L’ encefalopatia vascolare è comunque un’ opportunità per una prevenzione di lungo termine degli eventi cerebrovascolari e del declino cognitivo sopratutto con il trattamento dei fattori di rischio vascolare
•Talvolta è necessaria una Diagnosi Differenziale con malattie molto aggressive come la Sclerosi Multipla o le vasculiti (diagnosi differenziale sulla base dell’evolutività, dell’ estensione in relazione all’ età del soggetto , della morfologia delle lesioni, dei sintomi associati)
•Non sappiamo con certezza se l’ aspirina riduce il rischio di TIA/stroke o declino cognitivo in questi pazienti, ma sembra razionale usarla in base al profilo di rischio del paziente , dopo aver impostato un percorso di check up vascolare e il trattamento dei fattori di rischio stessi
•Un follow up del neuroimaging di lungo termine è consigliabile
Con l’ invecchiamento, il cervello va anche incontro ad atrofia, a perdita di massa neuronale 1
L’ atrofia cerebrale , in particolare dei poli temporali e del corno d’ Ammone , è una caratteristica della demenze degenerative, e tra questa in particolare dell’ Alzheimer.
Questa ultima è una proteinopatia duale (amiloide e tau) caratterizzata dalla coesistenza di aggregati extra-cellulari di Aβ42 e Aβ40 fibrille, che formano le placche neuritiche, e da aggregati intra-cellulari di tau iper-fosforilata (P-tau), chiamati neuro-fibrillary tangles (NFTs) 2.
•Il processo patologico inizia decadi prima della comparsa dei sintomi, con l’ accumulo di amiloide, poi di tau, poi compare la neuro-degenerazione (atrofia al neuroimaging) e infine la sintomatologia
•Tutto questo è monitorabile nel tempo con il neuroimaging molecolare e strutturale
•Particolari profili cognitivi (deficit cognitivi focali + deficit di memoria; minor funzionamento del default mode network al neuroimaging funzionale, cosa che probabilmente corrisponde alla condizione del paziente «perso in un bicchier d’acqua»; sono alterate le competenze cognitive specifiche, non solo le funzioni esecutive)
•I disturbi motori assenti anche quando i sintomi cognitivi sono francamente evidenti; non c’è perdita del controllo sfinterico, anche se nei casi avanzati ci può essere un comportamento inappropriato
•Fattori di rischio genetico
• Nell’ Alzheimer autonosomico dominante (ADAD) ci sono mutazioni conosciute nei geni APP, presenilin-1 (PSEN1) and presenilin-2 (PSEN2), che contribuiscono direttamente a incrementare la produzione di Aβ42 delle formazioni amiloidee e dell’ infiammazione.
• L’ Alzheimer sporadico è una malattia complessa sul piano genetico, con la apolipoprotein E ε4 allele (APOE*ε4) come principale fattore di rischio. Gli omozigoti per questo allele hanno un rischio di Alzheimer aumentato di 15 volte, mentre gli eterozigoti per lo stesso alleale hanno un rischio di Alzheimer aumentato di 3 volte.
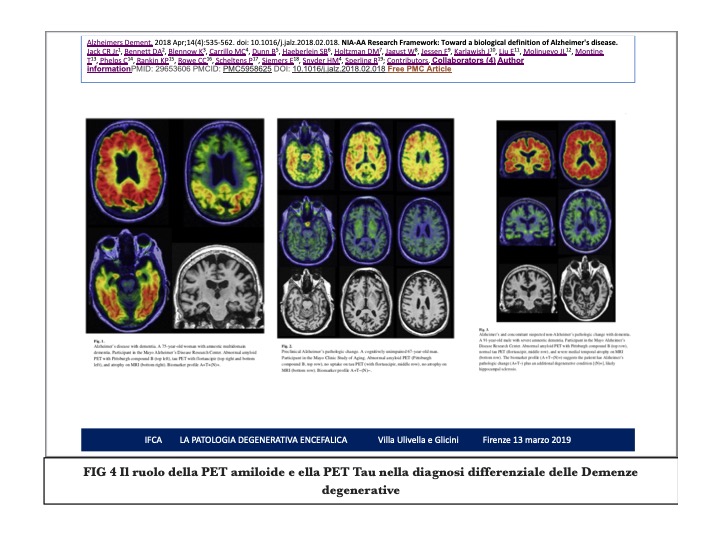
Gli accumuli di amiloide e tau sono documentabili con la PET, rispettivamente con Pittsburgh composto B e con Flortaucipir, come si vede nella figura (FIG 4). Nella figura si vedono le immagini di una soggetto con Alzheimer, che presenta positività per la presenza di accumuli di amilode , tau e atrofia cerebrale. Il secondo soggetto presenta solo accumuli di amiloide, non di tau , e non ha ancora atrofia né demenza. Può essere considerato un Alzheimer pre-clinico. Il terzo soggetto presenta severi accumuli di amiloide, severa atrofia e franca demenza , ma non accumuli di tau , e sicuramente è una Demenza non- Alzheimer.
In uno studio del 2014 3, si osservò che le persone cognitivamente normali
•sotto 60 anni non presentano né atrofia né accumuli di amiloide nel cervello nel 100% dei casi,
•tra 60 e 85 anni il quadro è più variegato. Solo il 21% dei soggetti è però ancora senza atrofia né accumuli di amiloide; il 20% presenta segni di depositi di amiloide senza atrofia (possibile Alzheimer pre-clinico); il 34% ha depositi di amiloide e atrofia, anche se è asintomatico (possibile Alzheimer asintomatico) ; infine il 25% presenta segni di patologia non Alzheimer (c’è l’ atrofia ma non l’ accumulo di amiloide).
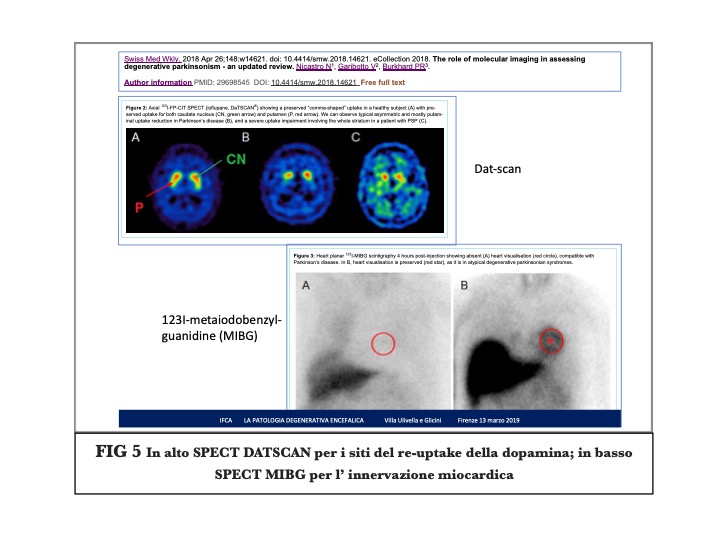
La figura successiva FIG. 5 mostra altre possibilità dell’ immagine molecolare nelle patologie degenerative dell’ encefalo.
Possiamo vedere con la SPECT-DATSCAN (ioflupane) la riduzione dei siti di uptake della dopamina nel putamen, o diffusamente in tutto lo striato, anche nel nucleo caudato nella Paralisi sopra-nucleare progressiva.
Ancora più suggestiva la completa mancanza di innervazione autonomia del cuore nel Parkinson (SPECT con 123I-metaiodobenzyl- guanidine, MIBG).
Anche nel Parkinson c’è un accumulo di una proteina patologica, la sinucleina.
La figura (FIG 6) mostra come molte patologie degenerative note dell’ encefalo presentano accumuli in vario grado e combinazione di queste tre proteine.

Cosa possiamo fare per queste patologie?
•Alzheimer: farmaci specifici (donepezil, rivastigmina, memantina) e la vecchia citicolina , oltre che le terapie socializzanti e di stimolo cognitivo
•Demenza vascolare: il trattamento tempestivo dei fattori di rischio
cerebrovascolari (diabete, ipertensione arteriosa, ipercolesterolemia , cardiopatie, ateromasia della carotide, fumo) può cambiare il destino di queste persone e rallentare la progressione anche nei soggetti sintomatici; uso degli antiaggreganti; citicolina e terapie socializzanti e di stimolo cognitivo
•Parkinson: Farmaci dopaminergici e dopa, con ottimi risultati sul Parkinson, molto minori su Parkinson- demenza e su altri parkinsonismi degenerativi; FKT mirata al cammino e postura; socializzazione
DEMENZA, DELIRIUM E IDROCEFALO NORMO-TESO
Oltre alla patologia encefalica vascolare e degenerativa, di cui abbiamo parlato finora, ci sono altre cause di demenza, e altri processi patologici encefalici, che possono provocare demenza o comunque alterazioni cognitive e/o della marcia e che vanno considerati nella diagnosi differenziale alle più comuni patologie vascolari e neuro-degenerative dell’ encefalo.
IL Delirium è una encefalopatia con compromissione delle funzioni cognitive e spesso anche motorie, acuta/subacuta, che può manifestarsi in un soggetto precedentemente normale , oppure con una preesistente encefalopatia di qualsiasi natura. (TAB. 2).

Qualsiasi perturbazione dell’equilibrio, dell’omeostasi del sistema nervoso centrale può scatenare il delirium: un evento vascolare/vasculitico, tossico-metabolico-carenziale, condizioni interimistiche come disidratazione e febbre, un evento traumatico, un intervento chirurgico e/o un’ anestesia, una crisi epilettica, o un infezione sistemica; il delirium può anche essere complicazione del decorso di un tumore endocranico.
Il delirium e la demenza sono due entità cliniche del tutto distinte , seppure possono coesistere. Nel delirium il soggetto è in stato confusionale, con vigilanza ridotta, e può essere anche in pericolo acuto-subacuto di vita, se le cause del delirium non vengono tempestivamente coperte e rimosse. In quest’ultimo caso si può avere anche un ottimo recupero sia delle condizioni fisiche che cognitive del paziente. Nel caso riportato in FIG 7, il delirium era dovuto alla comparsa di una pachi-meningite reattiva post-meningoencefalitica, in un soggetto che aveva già prima una modesta compromissione cognitiva su base neurodegenerativa.
Altre situazioni che hanno causato quadri di Delirium sono mostrate nella tabella 4.
Tra queste l’ encefalopatia di Wernicke da deficit di B1 4 , il cui quadro RM è riportato nella FIG . 8, anch’ essa proveniente dal citato articolo di Sechi e Serra del 2007 su Lancet Neurology.




L’ Idrocefalo Normo-teso è una condizione cronica, del soggetto anziano, determinata da un’ alterazione della dinamica liquorale, con dilatazione dei ventricoli cerebrali e tradizionalmente associata ad una triade sintomatologia , caratterizzata da disturbo del cammino (aprassia/atassia), disturbo cognitivo, incontinenza vescicale.
L’ idrocefalo si forma per uno squilibrio tra produzione e riassorbimento del liquor, che porta ad un abnorme dilatazione ventricolare e a un aumento della pressione intra-cranica. Ne può conseguire stravaso del liquor dal sistema ventricolare all’ interno del tessuto cerebrale, e successivo danno degenerativo-atrofico del tessuto nervoso stesso. L’ ampiezza del III ventricolo aumenta così che modifica la sua forma da quella a fessura a quella a pallone. Gli spazi liquorali esterni al contrario si assottigliano, al vertice (non a livello della scissura temporale, dove anzi possono essere sproporzionatamente ampi).
L’ Indice di Evans è usato nella pratica clinica per quantificare la dilatazione ventricolare nell’ adulto: un valore > 0.3 è significativo per idrocefalo.
Le alterazioni della sostanza bianca peri-ventricolare indotte dallo stravaso di liquor non sono distinguibili alla RM encefalo dalle alterazioni della sostanza bianca prodotte dall’ invecchiamento e sopratutto dalla leuco-araiosi. Le alterazioni della sostanza bianca peri-ventricolare correlate all’ idrocefalo sono di solito sottili (<10mm) sulle sezioni assiali, e il loro spessore decresce antero-posteriormente. In caso di idrocefalo normoteso è anche possibile vedere il segnale di vuoto nell’ acquedotto del Silvio (FIG 10).

Si distinguono 4 tipi di Idrocefalo in relazione al meccanismo della alterazione della dinamica liquorale:
1.ostruttivo o non comunicante;
2.da deficit di riassorbimento;
3.da iperproduzione;
4.normoteso
L’ Idrocefalo Ostruttivo, o non comunicante è causato da un’ ostruzione delle vie di deflusso liquorale.
1.Una lesione nella regione del foro del Monroe può provocare una dilatazione bilaterale o unilaterale dei ventricoli laterali . Il caso più comune è una ciste colloide.
2. Una stenosi acquisita dell’ acquedotto, su base infiammatoria o infettiva o malformativa/espansiva
3.La lesione ostruttiva può essere a livello del IV ventricolo o del form magno, come ad es per un infarto cerebellare o nella Sindrome di Arnold - Chiari.
L’ idrocefalo da mancato riassorbimento di solito interessa ugualmente tutto il sistema ventricolare (idrocefalo comunicante). Può conseguire ad una emorragia subaracnoidea o ad altri eventi emorragici, anche traumatici, oppure a meningismo cronico nel corso di malattie neoplastiche (in questo caso la RM mostra impregnazione marcata delle meningi dopo contrasto).
L’ idrocefalo ipersecretivo dipende da una produzione eccessiva di liquor causata di solito da un papilloma del plesso.
L’ idrocefalo idiopatico normoteso (INPH = idiopatic normal pressure hydrocephalus) è un tipo speciale di idrocefalo comunicante, che si manifesta nell’ adulto, durante l’ invecchiamento. Esso progredisce lentamente, con nessuno o scarso aumento della pressione endocranica, e si associa di solito a uno o più dei sintomi compresi della triade caratteristica (Triade di Hakim), che sono disturbi del cammino, cognitivi e del controllo vescicale.
L’ idrocefalo normo-teso ha di solito una storia molto lunga in ogni singolo paziente. L’ ipotesi patogenetica più accreditata è che, con il tempo, la capacità di deflusso del liquor, attraverso il sistema glimfatico cerebrale, si riduca progressivamente, questo anche per le alterazioni micro-strutturali del parenchima nervoso stesso (micro-ischemie , alterazioni della sostanza bianca), e che tutto ciò comporti un graduale aumento del volume dei ventricoli cerebrali. Il cervello (contenuto in una scatola cranica rigida) si deve adattare alle continue variazioni pulsatili del battito cardiaco (durante la sistole e diastole, il sangue entra nel cranio, mentre il liquor ne esce). Questa capacità di risposta immediata all’ iper-afflusso sistolico (elastanza) si riduce con l’ invecchiamento , in concomitanza anche con il ridotto deflusso del liquor attraverso il sistema glinfatico . Tutto ciò comporta un lento aumento del liquor all’ interno del sistema ventricolare cerebrale.
In alcuni casi una patologia cerebrale infantile (idrocefalo congenito) potrebbe precedere l’ evoluzione in età anziana verso un idrocefalo normo-teso.
La patogenesi dell’ idrocefalo normo-teso idiopatico potrebbe essere correlata in gran parte a disfunzione delle così dette vie glinfatiche (gliali - linfatiche), identificate finora nei roditori. Questa via linfatica permette un flusso di liquor lungo gli spazi perivascolari e poi nell’ interstizio del tessuto cerebrale, in correlazione con i canali per l’ acqua, aquaporina 4 (AQP4). La via suddetta quindi raggiunge gli spazi perivenulari e infine i vasi linfatici meningei. Questa via funziona sopratutto durante il sonno notturno.
La RM con agenti di contrasto permette di visualizzare questo sistema anche negli umani, e alterazioni dell’ espressione di AQP4 o ridotto deflusso nelle vie linfatiche cerebrali sarebbero stati osservati nell’ idrocefalo normo-teso5.
Nei pazienti con idrocefalo normo-teso, in un primo periodo o fase della malattia, il cervello già spinto contro contro la superficie intern del cranio reagisce vigorosamente all’ aumento dell’ afflusso di sangue durante la sistole, e così si instaura una condizione di flusso iperdinamico attraverso l’ acquedotto del Silvio (misurazione dello strofe volume con la RM). In una seconda fase, con il sopravvenire del danno parenchimale , e della perdita dell’ elastanza da parte del cervello, questo stato iperdinamico del flusso liquorale attraverso l’ acquedotto del Silvio recede. La condizione di flusso liquorale iperdinamico attraverso l’ acquedotto del Silvio è il miglior indice prognostico dell’ esito post-shunt chirurgico, inquinato è indirettamente anche una misura dell’ integrità del parenchima cerebrale. L’ indicazione allo shunt si pone solo quando lo strofe volume è almeno 2x il valore normale 6.
Nella valutazione pre-shunt, sono di comune uso vari test di sottrazione liquorale, lombare o craniale, e successiva valutazione del miglioramento clinico. In realtà c’è sufficiente evidenza che l’ unico test attendibile è in realtà il test di infusione intra-ventricolare di alcuni cc di fisiologica, che può valutare appunto l’ elastanza residua cerebrale. Un rapido e brusco incremento della pressione liquorale oltre un certo limite è correlato con l’ indicazione e la prognosi dell’ intervento.
In linea generale, il quadro di idrocefalo normo-teso è associato nella maggior parte dei pazienti anziani , che vengono all’ osservazione, ad altre encefalopatie degenerative o vascolari. Anche qualora si riesca a definire che l’ idrocefalo normo-teso gioca un qualche ruolo nel quadro clinico in atto, non si può escludere che il decorso a medio termine (i primi anni successivi all’ intervento) mostri di nuovo un peggioramento clinico in relazione alla progressione della patologie vascolari/degenerative concomitanti. Secondo uno studio del 2017, i benefici post-shunt persistevano dopo 3 anni solo in 1/3 pazienti operati, e in almeno 1/4 degli operati veniva successivamente evidenziata una chiara encefalopatia degenerativa non valutata in un primo momento.


La sintesi di quanto sopra è che: dunque:
1.Pazienti anziani che hanno disturbi di vario tipo della marcia e cognitivi, e dilatazione ventricolare al neuroimaging , possono essere valutati attentamente su base clinica e al neuroimaging, per definire la natura dei loro sintomi
2.Molti di loro presentano pluri-patologie e vario grado di atrofia/leuco-araiosi , e quindi il ruolo della aumentata pressione liquorale nella genesi dei loro sintomi, seppure presente, può essere molto limitato, così come potrebbero essere scarsi e di breve durata i vantaggi di un eventuale intervento di derivazione.
3.Il candidato ideale è quello in cui il neuroimaging e la valutazione clinica indirizzano chiaramente verso la presenza di un idrocefalo normo-teso come responsabile principale della sintomatologia (scarsa o assente co-patologia, stroke volume almeno raddoppiato, atrofia assente o limitata). E’ possibile che il test di infusione pre-shunt riesca a selezionare molto accuratamente la casistica di coloro che potranno trarre vantaggio dall’intervento.
****
BIBLIOGRAFIA